⚠️ Avertissement informatif : Cet article est rédigé à des fins d’information scientifique générale. Il ne constitue pas un avis médical et ne remplace en aucun cas une consultation avec un professionnel de santé. Tout traitement médicamenteux, y compris les agonistes des récepteurs GLP-1, doit être prescrit et suivi par un médecin.
Qu’est-ce que l’orforglipron ?
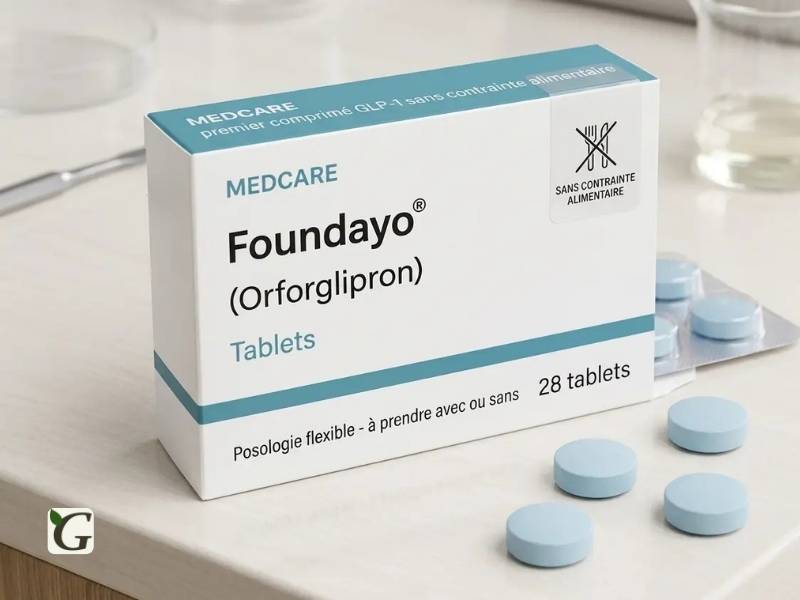
L’orforglipron est une molécule développée par le laboratoire pharmaceutique américain Eli Lilly, initialement découverte par Chugai Pharmaceutical et licenciée par Lilly en 2018. Commercialisé sous le nom de marque Foundayo aux États-Unis, il appartient à la classe des agonistes des récepteurs GLP-1 (Glucagon-like peptide-1) — la même famille que le sémaglutide (Wegovy, Ozempic) ou le tirzépatide (Mounjaro, Zepbound).
Sa grande particularité : c’est une petite molécule non peptidique, administrée sous forme de comprimé oral quotidien, qui peut être prise à n’importe quel moment de la journée, sans restriction liée aux repas ni à l’eau. C’est une différence majeure par rapport aux traitements injectables hebdomadaires, mais aussi par rapport à la pilule de sémaglutide oral (Wegovy pill), qui doit être prise le matin à jeun, 30 minutes avant tout aliment ou boisson.
💊 En résumé : même mécanisme d’action que les injections GLP-1, mais sous forme de comprimé souple d’utilisation.
Mécanisme d’action
Comme tous les agonistes GLP-1, l’orforglipron imite l’action de l’hormone GLP-1, naturellement sécrétée par l’intestin après les repas. Cette hormone agit sur plusieurs mécanismes :
- Ralentissement de la vidange gastrique → sentiment de satiété prolongé
- Réduction de l’appétit via des signaux envoyés au cerveau (hypothalamus)
- Amélioration de la régulation de la glycémie en stimulant la sécrétion d’insuline
- Réduction du stockage des graisses viscérales
Ce qui distingue l’orforglipron des autres GLP-1 disponibles, c’est sa structure chimique de petite molécule synthétique (non peptidique), ce qui permet sa prise orale sans dégradation digestive — problème qui limitait historiquement les GLP-1 administrés par voie orale.
Communauté Glukoa
Rejoignez 120+ patients
sous traitement GLP-1
Alertes prix · Recettes adaptées
Guide médical · Sans spam
Sans engagement · RGPD · Désabonnement en 1 clic
Les études cliniques de référence
🔬 ATTAIN-1 — Obésité sans diabète
L’étude pivot ATTAIN-1 est une étude de phase 3, multinationale, randomisée en double aveugle, menée sur 3 127 adultes obèses sans diabète. Publiée le 16 septembre 2025 dans le New England Journal of Medicine (DOI : 10.1056/NEJMoa2511774), elle constitue la référence scientifique principale pour ce médicament.
Les participants ont reçu pendant 72 semaines soit un placebo, soit l’une des trois doses d’orforglipron (6 mg, 12 mg ou 36 mg par jour), en complément d’une alimentation équilibrée et d’une activité physique.
Résultats à 72 semaines (perte de poids moyenne) :
| Dose | Perte de poids moyenne | ≥ 10 % de perte |
|---|---|---|
| Placebo | −2,1 % | 12,9 % des patients |
| 6 mg | −7,5 % | — |
| 12 mg | −8,4 % | — |
| 36 mg | −11,2 % | 54,6 % des patients |
Parmi les participants ayant complété le traitement, la dose maximale a conduit à une perte moyenne de 12,4 % du poids corporel, soit environ 12,4 kg (27,3 livres).
Effets cardiométaboliques observés :
- Réduction significative du tour de taille
- Amélioration de la pression artérielle systolique
- Baisse des triglycérides et du cholestérol non-HDL
- Parmi les 1 127 participants en prédiabète au début de l’étude, jusqu’à 91 % de ceux sous orforglipron 36 mg ont retrouvé une glycémie quasi-normale (vs 42 % sous placebo)
📖 Source : New England Journal of Medicine, 16 sept. 2025 — financé par Eli Lilly
🔬 ATTAIN-2 — Obésité avec diabète de type 2
L’étude ATTAIN-2, publiée dans The Lancet en novembre 2025, a évalué l’orforglipron chez des patients obèses ou en surpoids avec diabète de type 2. À la dose de 36 mg, la perte de poids moyenne atteignait 10,5 % à 72 semaines (vs 2,2 % sous placebo), avec une réduction de l’HbA1c de 1,3 à 1,8 %.
📖 Source : The Lancet, novembre 2025 — programme ATTAIN d’Eli Lilly
🔬 ACHIEVE-3 — Comparaison avec le sémaglutide oral
L’étude ACHIEVE-3, publiée dans The Lancet le 26 février 2026, a comparé directement l’orforglipron au sémaglutide oral (Rybelsus) chez des adultes avec diabète de type 2. L’orforglipron a démontré sa non-infériorité en termes de contrôle glycémique — une donnée importante pour positionner ce traitement comme alternative crédible dans l’arsenal thérapeutique.
📖 Source : The Lancet, 26 févr. 2026
Approbation réglementaire
🇺🇸 FDA — Approuvé le 1er avril 2026
Le 1er avril 2026, la FDA (Food and Drug Administration) américaine a officiellement approuvé le Foundayo (orforglipron) pour la prise en charge du poids chez les adultes obèses ou en surpoids avec au moins une comorbidité liée au poids, en complément d’un régime hypocalorique et d’une activité physique accrue.
Cette approbation est historique à plusieurs titres :
- Elle a été accordée 50 jours après le dépôt du dossier — soit l’approbation la plus rapide pour une nouvelle entité moléculaire depuis 2002
- Elle s’inscrit dans le programme Commissioner’s National Priority Voucher (CNPV) de la FDA, visant à accélérer l’accès aux traitements répondant à des priorités de santé publique
🇪🇺 Europe (EMA) — En cours d’évaluation
En France et en Europe, l’orforglipron ne dispose pas encore d’une autorisation de mise sur le marché (AMM). Eli Lilly a soumis des dossiers auprès des autorités sanitaires de plus de 40 pays, dont l’Agence Européenne des Médicaments (EMA). Aucune décision de remboursement par la Haute Autorité de Santé (HAS) n’a été rendue publique à ce stade.
📖 Source : Ma Santé, janvier 2026 — Le Quotidien du Médecin, avril 2026
Effets indésirables connus
Comme pour l’ensemble des agonistes du GLP-1, les effets indésirables sont principalement gastro-intestinaux et d’intensité légère à modérée :
- Nausées
- Diarrhées
- Constipation
- Vomissements
- Douleurs abdominales
- Céphalées
- Perte de cheveux (alopécie temporaire)
Les taux d’arrêt du traitement liés aux effets indésirables se situaient entre 5 et 10 % dans les essais cliniques — un niveau comparable aux autres GLP-1.
Contre-indications importantes :
L’orforglipron comporte une mise en garde concernant les tumeurs des cellules C thyroïdiennes (carcinome médullaire de la thyroïde). Il est contre-indiqué chez les personnes ayant des antécédents personnels ou familiaux de carcinome médullaire de la thyroïde ou de néoplasie endocrinienne multiple de type 2.
⚠️ L’association avec d’autres agonistes GLP-1 n’est pas recommandée.
📖 Source : AJMC (American Journal of Managed Care), avril 2026
Prix et accessibilité
🇺🇸 Prix aux États-Unis (à compter d’avril 2026)
| Profil patient | Coût mensuel estimé |
|---|---|
| Assuré (avec carte de réduction Lilly) | ~25 $/mois |
| Sans assurance — dose minimale | 149 $/mois |
| Sans assurance — dose maximale | jusqu’à 349 $/mois |
| Medicare Part D (dès juillet 2026) | ~50 $/mois |
À titre de comparaison, un mois de traitement avec Wegovy ou Zepbound en version injectable coûte entre 1 000 et 1 350 $ aux États-Unis sans assurance — ce qui fait de l’orforglipron une option significativement plus accessible.
📖 Sources : Info-Utiles.fr, avril 2026 — PharmExec, avril 2026
🇫🇷 Prix en France — Pas encore disponible
En France, aucun prix officiel n’a été communiqué, l’AMM européenne n’ayant pas encore été accordée. À titre indicatif, des analystes de marché (Business Insider) estimaient le coût potentiel dans une fourchette autour de 300 € par mois — comparable au Wegovy (300–350 €/mois hors remboursement).
La question du remboursement par l’Assurance maladie reste ouverte, dans un contexte où la HAS n’a pas encore tranché pour les traitements anti-obésité injectables existants (Wegovy).
📖 Source : Ma Santé, janvier 2026 — Meilleurtaux.com, novembre 2025
Ce que ça change pour les patients GLP-1
L’orforglipron ne rivalise pas encore en efficacité avec les injectables comme le tirzépatide (Zepbound) — le PDG d’Eli Lilly lui-même l’a reconnu publiquement. Mais il présente plusieurs avantages concrets :
✅ Forme comprimé → plus de piqûres, pas de chaîne du froid, facilité de transport
✅ Prise libre → aucune contrainte horaire ni alimentaire (contrairement au sémaglutide oral)
✅ Fabrication plus simple → petite molécule chimique, plus facile à produire à grande échelle que les peptides biologiques
✅ Prix potentiellement plus bas → bien en-dessous des injectables
✅ Transition facilitée → pour les patients déjà sous injectable souhaitant passer à une forme orale
Perspectives : au-delà de l’obésité
L’orforglipron fait l’objet d’études cliniques dans plusieurs autres pathologies :
- Diabète de type 2 (dossier EMA en cours)
- Apnée obstructive du sommeil
- Douleurs arthrosiques du genou
- Hypertension artérielle
- Maladies artérielles périphériques
- Incontinence urinaire d’effort
📖 Source : Le Quotidien du Médecin, avril 2026
💡 Conseil Glukoa — Spécifique GLP-1
Si vous êtes sous traitement GLP-1 (injectable ou oral) et que vous entendez parler de l’orforglipron, n’envisagez pas un changement de traitement sans l’avis de votre médecin. Les études montrent que l’arrêt brutal d’un GLP-1 entraîne une reprise d’environ 80 % du poids perdu dans les 6 mois. Toute transition entre molécules ou formes galéniques doit être planifiée et encadrée médicalement.
Sources citées
- New England Journal of Medicine — ATTAIN-1, 16 sept. 2025 → https://www.nejm.org/doi/full/10.1056/NEJMoa2511774
- FDA — Approbation Foundayo, 1er avril 2026 → https://www.fda.gov/news-events/press-announcements/fda-approves-first-new-molecular-entity-under-national-priority-voucher-program
- Eli Lilly — Page officielle orforglipron → https://www.lilly.com/news/stories/what-to-know-about-orforglipron
- The Lancet — ACHIEVE-3, 26 févr. 2026 → https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(26)00202-3/fulltext
- Le Quotidien du Médecin — Feu vert FDA, avril 2026 → https://www.lequotidiendumedecin.fr/actu-medicale/medicament/obesite-feu-vert-de-la-fda-pour-lorforglipron
- Centre de l’Obésité et de la Nutrition — Présentation clinique → https://www.centreobesite.fr/details-orforglipron+un+nouvel+espoir+oral+dans+le+traitement+de+l+obesite-620.html
- AJMC — Détails approbation FDA → https://www.ajmc.com/view/fda-approves-lilly-s-oral-glp-1-orforglipron-for-obesity
- Ma Santé — Disponibilité en France → https://ma-sante.news/obesite-bientot-un-comprime-minceur-sur-le-marche/
- 🔥 Mounjaro, Wegovy et la « Golden Dose » : ce que vous devez vraiment savoir
- 🤔 Orforglipron (Foundayo) : le premier comprimé GLP-1 sans contrainte alimentaire
- 😊 GLP-1 et peau : comprendre les effets cutanés de l’amaigrissement

- ☺️ Comment prendre le GLP-1 : guide complet selon votre forme galénique

- 😊 Compléments « GLP-1 » en gouttes, patches et dosettes : ce qu’il faut savoir avant d’acheter